

 海博微信公众号
海博微信公众号
 海博天猫旗舰店
海博天猫旗舰店


 海博微信公众号
海博微信公众号
 海博天猫旗舰店
海博天猫旗舰店




一、培养基用途
mCPC培养基用于致病性弧菌的选择性分离。
二、检验原理
蛋白胨、牛肉粉作为培养基中的基础营养物质,提供细菌生长所需的碳氮源、维生素和其他的生长因子;氯化钠维持培养基体系的渗透压平衡;多粘菌素B和多粘菌素E能抑制副溶血性弧菌和溶藻弧菌等非目标菌的生长;纤维二糖为可发酵的糖类;溴百里酚兰和甲酚红为pH指示剂;琼脂是培养基的凝固剂。本培养基一纤维二糖作为鉴别剂,创伤弧菌可发酵纤维二糖产酸显黄色。
三、培养基配方(g/L)
|
蛋白胨 |
10.0 |
| 氯化钠 | 20.0 |
| 琼脂 | 15.0 |
| 甲酚红 | 0.04 |
| 溴百里酚兰 | 0.04 |
| 牛肉粉 | 5.0 |
| pH值7.5-7.7 | 25℃ |
四、试验方法
1.称取本品5.0克,加热煮沸溶解90mL蒸馏水中,冷却到48-55℃时加入10%纤维二糖水溶液10mL和1支mCPC添加剂(多粘菌素E 40000units和多粘菌素B 10000units)混匀,倾入无菌空平皿,无需高压灭菌;
2.制备质控菌液;
3.目标菌(创伤弧菌):选择合适稀释度的质控菌液100μL,均匀涂布于待测培养基上,每一稀释度接种两个平板;非目标菌(特异性):使用1μL接种环挑取1环霍乱弧菌菌液,定性划线接种于待测平板;非目标菌(选择性):分别使用1μL接种环挑取1环副溶血性弧菌、大肠埃希氏菌和金黄色葡萄球菌菌液,在待测平板表面划六条平行线;
4.放置36±1℃需氧培养24-48小时,记录试验结果。
五、试验结果判断
接种以下质控菌株,放置36±1℃需氧培养24-48小时。
|
质控菌株 |
菌株编号 |
接种量(CFU) |
参比或计数培养基 |
方法 |
质控结果 |
其他特征 |
|
副溶血性弧菌 |
ATCC17802 |
/ |
/ |
半定量 |
G≤1 |
抑制 |
|
霍乱弧菌 |
/ |
/ |
/ |
定性 |
/ |
紫色菌落 |
|
创伤弧菌 |
ATCC27562 |
20-200 |
3%NaCl TSA |
定量 |
PR≥0.1 |
圆形扁平,中心不透明, 边缘透明的黄色菌落 |
|
大肠埃希氏菌 |
ATCC25922 |
/ |
/ |
半定量 |
G≤1 |
抑制 |
|
金黄色葡萄球菌 |
ATCC25923 |
/ |
/ |
半定量 |
G≤1 |
抑制 |
mCPC培养基质控结果:
 |
|
 |
|
 |
|
副溶血性弧菌 抑制 |
|
霍乱弧菌 紫色菌落 |
|
金黄色葡萄球菌 抑制 |
 |
|
|
|
 |
|
大肠埃希氏菌 抑制 |
|
|
|
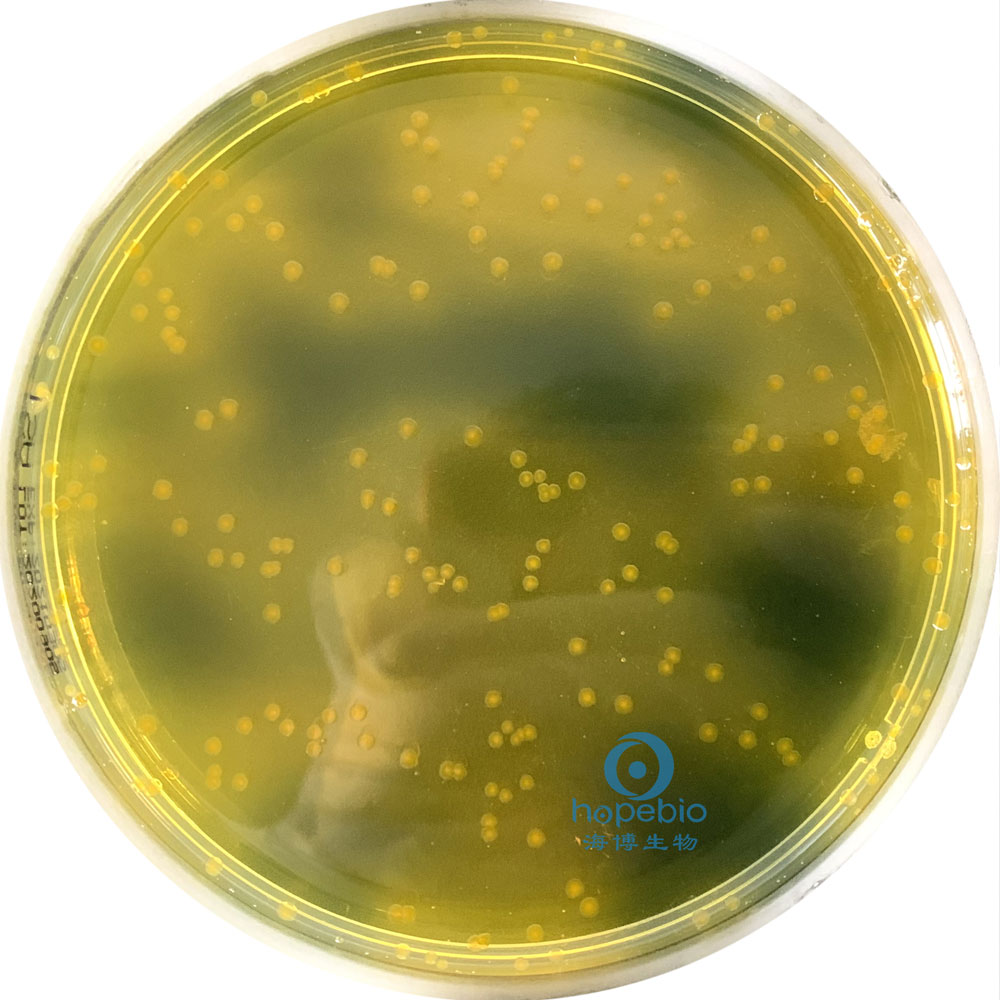
创伤弧菌 圆形扁平,中心不透明,边缘透明的黄色菌落 |
相关产品:
注:本文属海博生物原创,未经允许不得转载。
下一篇:克氏柠檬酸盐培养基原理和质控方法



