

 海博微信公众号
海博微信公众号
 海博天猫旗舰店
海博天猫旗舰店


 海博微信公众号
海博微信公众号
 海博天猫旗舰店
海博天猫旗舰店




药品微生物限度检查(以下简称微限)的目的是确定药品(含原料及辅料)是否污染微生物或其污染微生物的程度,将微生物的种类和数量限制在一定的范围之内或者不得检出,是保证用药的有效性、保障药品安全性的重要措施。也是衡量药品生产,流通以及使用全过程微生物控制水平的主要依据之一。科学技术的进步,药品生产工艺的提高以及人民对药品安全理念的不断提升,促使药品检验标准不断提高,微生物限度检查作为药品质量的安全性评价指标也不例外。我国的首版药典于1953年出版,但开展药品微生物污染检查工作始于1972年,《中国药典》(1995年版)初次收载了微生物限度检查法,2000年版首次收载了微生物限度标准,2015年版形成了较为完善的药品微生物控制标准体系,并解决了基本与美国药典等国际人用药品注册技术要求国际协调会(ICH)方案接轨。《中国药典》(2020年版)进一步促进了药品微生物实验室的管理与国际接轨,实现了微限检查由最终产品检验向过程控制的改变。为了提升药品微生物实验室的检验能力,选取了2019年1月至2020年12月期间实验室微限检查结果作为样本,对微限检查误差来源进行回顾性梳理,以期减少或避免误差出现的概率,保证微限检查结果的准确性。
1 资料与方法
1.1 资料
选取2019年1月-2020年12月,本实验室承担的药品微限检查共870批,其中片剂372批、丸剂187批、颗粒剂227批、口服液84批。对研究药品微限检查误差的相关文献进行检索,并分类整理。
1.2 方法
按照标准对870批药品进行微限检查,记录发生误差的情况,分析误差产生的来源并对检验中出现的误差进行统计,采用Microsoft Office Excel 2007进行整理分析,以回顾性分析的方法探究出现误差的影响因素,了解其分布情况。同时对比文献研究数据,观察本实验室与其他地市级药品检验机构的差异,以期在未来的工作中减少误差发生率。
2 结果
对上述870批药品微限检查的统计结果显示,有42批次(4.8%)因受到操作环境、供试液制备等因素影响导致检验结果出现偏差。影响因素、误差例数及占比情况见表1。
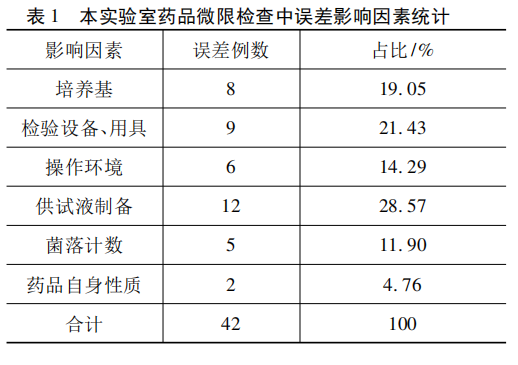
通过中国知网数据库查阅文献资料,选取部分高同质性的药品检验机构微生物实验室的文献资料,研究统计并进行综合分析,共1180例误差数据,详见表2。

表1和表2对比情况见图1。可以看出,药品微限检查误差中,影响因素主要来自六个方面,其中供试液制备时出现误差比例最高,其次是培养基,另外依次是检验设备及用具、操作环境、菌落计数和药品自身性质。本实验室和其他地市实验室统计结果基本一致。
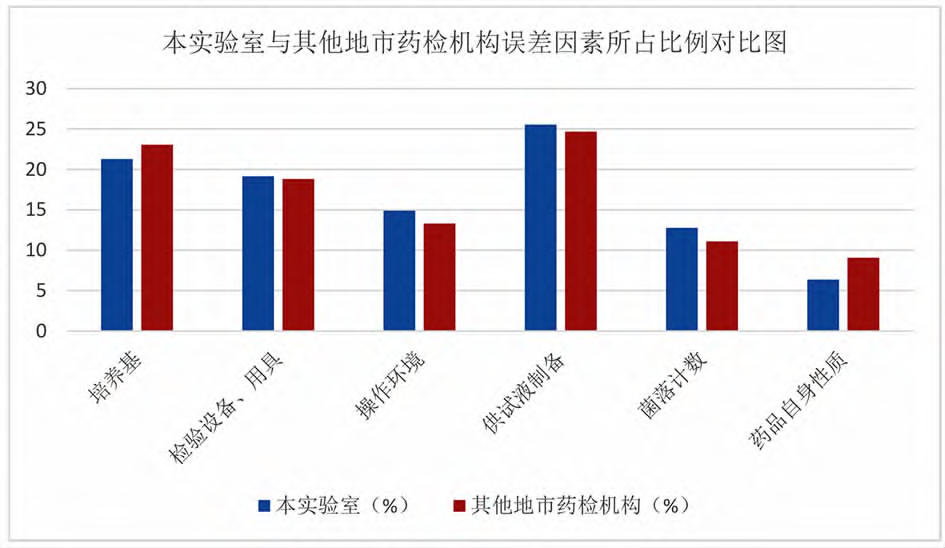
图1本实验室与其他地市药检机构误差影响因素所占比例对比图
3 误差影响因素的分析及探讨
药品微限检查目前最常用的方法是生物学检验技术,该技术操作程序较为繁琐、检验流程要求紧密严格,检验周期较长,导致出现干扰因素的环节较多,容易导致检验结果出现误差。因此,总结分析误差影响因素,在今后的检验工作中给予充分关注,可以减少误差出现的概率,保证检验结果的准确性与可靠性。
3.1 供试液制备
供试液制备是误差发生的主要因素,该工作目前主要由检验人员完成,没有自动化仪器设备可以替代。因此,检验人员的专业素养、理论知识、操作技能和工作经验是严格规范操作、保证结果准确性的基础。
供试液制备时应保证样品的真实污染状态,既不能杀死样品本身污染的微生物,也不能污染样品,还要避免操作不当导致样品污染实验环境。要通过方法适用性检查,保证供试液不具有或者消除其杀菌及抑菌活性。在注皿之前,应保证样品分散均匀,避免吸取供试液的沉淀物或上清液造成结果偏离。为防止细菌增殖,制备过程要稳、准、快,从供试液制备到倾注培养基整个操作过程应严格控制在1小时内,避免时间过长对检验结果造成影响。
鉴于药检机构成立时间早,人员更新慢,专业结构不合理,人员老化较为严重,现有工作人员大部分经历了多版药典的实施。有些人员学习能力较差,学习意识淡泊,不能及时跟进检验标准的变化,不能有效理解新版药典微限检查的操作要求,容易在操作中出现失误,最终导致出现错误的结果。主要表现在以下几个方面:一是有些药检机构认为微限检查不使用大型精密仪器,检验方法较为单一,对人员和技术要求不高。在人员配置时将非微生物学专业毕业的人员、无相关微限检查工作经历的人员安排到微限检查岗位; 二是药检机构中相比较于理化检验人员,微限检查人员较少,考虑到培训成本,“请进来”的培训几乎没有。除了技术骨干极少的外出培训机会,大多靠检验人员自学,学习的自觉性、学习的效果均难以追踪考核; 三是上岗考核流于形式。对于新进人员或者转岗人员,上岗考试基本以笔试为主,形式大于内容,对操作技能重视不够。
3.2 培养基
培养基是微生物检验的基础,直接影响微生物检验结果。目前,大部分实验室使用商品化培养基,收到培养基后应对品名、批号、生产厂家及有效期等进行初步验收,使用前应进行适用性检查,适用性检查符合要求方可使用。开瓶时应注明开瓶日期和经验证的有效期,一旦发现受潮结块等现象,应立即停止使用。使用时应按标签标识的说明进行配制,配制时应充分溶解,一般采用湿热灭菌法。为保证灭菌时既不破坏有效成分,又要保证灭菌彻底,需按照经验证的灭菌条件操作。应确定每批培养基灭菌后的pH值的范围(冷却至25℃左右测定),温度过高测定pH值时颜色反应可能有误差。灭菌后的培养基pH值如果测定时超出范围,不便调整。因此,建议实验室在灭菌前测定培养基pH值,一旦超出范围,应缓慢滴加适宜的碱液或者酸液进行调整,添加过量导致再矫正时,培养基的灵敏性可能降低,影响菌落生长。
陈晓燕指出灭菌后的培养基可以在2~8℃放置60天,但因为各实验室温度、相对湿度、冰箱性能等控制条件有差异,如要延长保存时间,需要在本实验室开展验证。因此,建议临用新制,避免培养基保存期间导致的促生长能力、抑制能力及指示特性下降。
3.3 检验设备及用具
仪器设备应定期进行检定/校准,不得使用超过检定/校准周期的仪器设备。仪器设备运行期间,应严格按照维护计划执行,以保持良好的工作状态。影响实验结果准确性的关键设备有高压灭菌器、冰箱以及培养箱,在运行过程中对温度、压力等关键参数要连续观测,并做好记录,尤其是高压锅,遇到仪器出现故障时要及时发现并处置,避免出现意外伤害事故。本实验室曾有一台高压灭菌器在达到灭菌条件和灭菌时间后,仍然保持高温高压,为防止意外,只能强制断电中止设备运行,本次灭菌的培养基作废弃物处理。
检验中用到的玻璃仪器等用具均需进行灭菌,目前大部分实验室改用一次性无菌培养皿,省去了培养皿清洁和灭菌的繁琐。但使用一次性无菌培养皿前,尤其在更换生产厂家后,应注意验收,可选用少量与库存培养皿进行对比试验。本实验室曾在某次实验时出现多批不同品种样品菌落数超标,同时阴性对照有菌落生长,当次实验结果全部作废。启动偏差调查,经回顾性分析和反复讨论,考虑是新到货培养皿的问题。使用原库存的培养皿进行对比验证后,确认是培养皿不合格,随即联系供应部门对该批次培养皿进行了退换,同时建议供应部门加强对供应商的评估。
3.4 操作环境
为降低或避免交叉污染,微限检查应在不低于D级背景下的生物安全柜或B级洁净区域内进行,且操作区域内应为单向流空气。为保持环境的适宜性和有效性,年初应制定环境监测计划,定期监测浮游菌、沉降菌、压差等重要参数。空调洁净系统长时间运行后,初效、高效过滤网更换不及时,会有洁净度不符合要求的风险。检验人员应具有无菌意识,将无菌观念铭记在心,落实在细节处。
检验前要做好充分的准备工作,将所需物品全部放进无菌室,检验过程中严禁进出实验室取用实验用品。在无菌室内检验用具要保存在固定位置,杜绝随意移动,无关物品禁止入内。生物安全柜应保持台面清洁,使用前按规定进行消毒,还要定期委托有资质的第三方实验室进行校准,对滤网等关键配件要定期清理或更换。实验中人员是洁净室内主要的发尘源,单位面积内人员越多,对实验环境影响越大,实验结果的可信度越差。因此,实验时无关人员禁止入内,同时检验操作应平稳有序,严禁人员频繁走动、接打电话,以避免搅动空气中的尘埃粒子,影响检验结果。
3.5 菌落计数
菌落计数方法首先要考虑方法的选择及确认。一般首选操作过程简单的方法,常用的是低稀释级(1∶10稀释液)平皿倾注法,从而减少操作繁杂带来误差或者损伤微生物。其次选用增加稀释倍数或培养基体积、添加中和剂或灭活剂等去除或灭活供试液的抗菌活性,再次选择薄膜过滤法,或者上述几种方法联用。最可能数法因为精密度及准确度较差一般不选用。无论采取哪种方法,均要考虑所添加的表面活性剂、中和剂、灭活剂等试剂对微生物无毒性,同时确认所用试剂的相容性,避免发生反应影响检验结果。实验中一定要进行阴性对照试验,在出现菌落生长时,便于区分药品自身情况还是操作环境等其他因素影响。
菌落计数时一般通过直接观察,在平皿的背面进行菌落计数,计数时应注意平皿边缘生长的菌落,同时注意区分菌落和颗粒物、胶囊壳碎片等,可借助放大镜、低倍显微镜观察,必要时挑取可疑物进行涂片镜检。
药典中规定的有需氧菌总数、霉菌和酵母菌总数、控制菌检查。微生物广泛存在于自然界中,药品中污染微生物的种类有可能不在其规定范围内。出现不明菌落时,应进行鉴定,确定污染的原因并及时采取预防措施。一旦确定是样品自身原因,应立即上报监管部门,避免发生药害事件。
3.6 药品自身性质
合格的药品是生产出来的,不是检验出来的。在药物生产、运输、存储过程中,都有可能会污染微生物。药品的生产环境、工艺、设备、原料及辅料、质量控制方法及水平和生产人员等均有可能带来药品微生物的污染。
实验室收到样品后,首先应做好唯一性标识,避免样品混淆,尤其针对三同样品(同品种同厂家同批号)。应严格按照说明书上记载的贮藏方式保存样品,最大限度保持样品原始状态,避免样品贮藏条件比如相对湿度过高、温度过高等不符合要求导致的微生物污染。
药品中可能含有防腐剂,如果防腐剂未被中和或灭活,平板计数结果往往会受到影响,如低稀释级菌落生长数量较少,而高稀释级菌落生长数量反而增大,遇此情况应重复试验,确定是药品自身性质影响还是操作技术造成的误差。样品的给药途径、抑菌程度等因素会影响检验方法的选择,不同的检验方法又可能带来不同的误差来源。
4 讨论及改进措施
针对误差因素的分析,有条件的实验室应配备微生物及相关专业毕业、有较高专业知识水平的人员。检验人员上岗前,必须进行严格的岗前培训,要熟练操作仪器设备,明确无菌操作要求,按规定制备培养基、洁净室的消毒、培养基及废弃物的灭菌、平板制作、菌落的计数方法、菌落的鉴定、菌种的保藏及传代、洁净室的微生物监测等。要对检验人员加强生物安全培训,熟悉安全操作规范和灭菌消毒知识,保证自身安全的同时,也能有效防止实验室被微生物污染。
出现不合格结果时,应及时启动偏差调查,评估是样品的原因还是实验室误差。积极参加外部组织的能力验证等方式外,可在实验室内部开展盲样检测等活动来考察检验技能和水平。当开展新项目、使用新方法或新技术时,检测开始前对其操作技能要进行专项评估确认。
药典中的微限检查对象是活的微生物,而药品中污染的微生物具有分布不均匀性。同一批次药品可能部分被污染;被污染的药品中,污染微生物的数量可能也不一致;被污染药品微生物种类可能比较复杂,也可能比较单一。微生物具有族团性,其大小及紧密程度具有遗传性,族团的分化性差异极大,进一步强化分布不均匀性。针对上述特点,抽样时应严格遵守抽样指导原则,保证样品具有代表性。
要强化检验人员对微限检查全过程的质量控制意识,做到以药典指导原则为纲,落到细处,落到实处。建立本实验室微限检查的标准操作规程,使微限检查逐步趋向规范化,标准化,既要防止假阳性结果,更要避免假阴性结果,应客观反映出药品中微生物污染程度,确保检验结果的准确性,为药品安全有效提供技术支撑。
来源:菏泽市食品药品检验检测研究院 曹鲁娜 毕言锋 任仲丽 毕天琛 李怀伟
提醒:本文章所有内容均来源网络,仅用于学习交流,若有侵权内容,请及时联系删除或修改,特此声明!
上一篇:基因突变的类型
下一篇:微生物培养基主要成分综述
| 相关文章: | ||



