

 海博微信公众号
海博微信公众号
 海博天猫旗舰店
海博天猫旗舰店


 海博微信公众号
海博微信公众号
 海博天猫旗舰店
海博天猫旗舰店




作者:刘焱斌1,刘涛2,崔跃2,王博3,罗凤鸣3
1. 四川大学华西医院感染性疾病中心(四川成都 610041)
2. 武汉市红十字会医院(湖北武汉 430015)
3. 四川大学华西医院呼吸与危重症医学科(四川成都 610041)
摘 要
【目的】 探讨新型冠状病毒肺炎核酸检测中相对方便安全及敏感度高的方法。方法 对武汉市红十字会医院100例新型冠状病毒肺炎病例同时留取咽拭子和鼻拭子。比较两种方法取样后样本核酸检测的阳性率。
【结果】 咽拭子取样标本新型冠状病毒核酸阳性检出率54%;而鼻拭子取样标本的病毒核酸阳性率89%。
【结论】 新型冠状病毒肺炎患者取鼻拭子进行核酸检测的阳性检出率具有明显优势。临床应尽可能使用鼻拭子而非咽拭子作为新型冠状病毒肺炎患者的优选筛检方式。
【关键词】 新型冠状病毒肺炎;咽拭子;鼻拭子;核酸检测
2019年12月以来,新型冠状病毒肺炎在武汉爆发并席卷全国,截止2020年2月17日,国家卫生健康委官方网站发布确诊病例70640例(含临床诊断病例)。随着医学科技的发展,分子生物学技术被广泛地应用于呼吸道病毒感染快速检测和精确诊断[1]。而在该病的诊断方面鼻咽拭子的新型冠状病毒核酸检测是最重要的确诊标准。
在援鄂诊治新型冠状病毒肺炎的临床实践中, 常出现有患者咽拭子核酸检测阴性后再次复查鼻拭子核酸检测又呈阳性的现象。在应用PCR技术进行检测时,呼吸道病毒在检测过程中,标本不同可能会影响检测阳性率的偏差[2]。为了解两种拭子在新型冠状病毒核酸检测中的区别以及引导临床正确实践。并且能减少仍具传染性患者离开隔离条件而导致该病毒进一步传染扩散。我们观察了临床100例患者的鼻拭子及咽拭子的核酸检测结果,供今后临床实践参考。
1、资料与方法
1.1 临床资料
选择2020年2月10日-2月21日在武汉某医院发热门诊及隔离病房住院患者共100例,其中发热门诊取样20例,隔离病房住院患者80例次。男性56例,女性44例,年龄22-81岁,平均58岁。患者入选标准以国家卫生健康委员会发布的《新型冠状病毒感染的肺炎诊疗方案(试行第四版)》中符合疑似及确诊病例诊断标准进行筛选。
1.2 方法
1.2.1 拭子选择
咽拭子为江苏康健医疗用品公司生产与细胞裂解液配套的灭菌一次性塑料杆棉拭子;鼻拭子为意大利COPAN公司产一次性塑料杆尼龙植绒拭子(图1)。

图1
1.2.2 采样方法
患者在留取新型冠状病毒核酸检测取样时,同时进行咽拭子和鼻拭子采样。
咽拭子采样时患者用清水漱口,然后让患者张口发"啊"音,必要时使用压舌板。取出灭菌棉拭子轻柔、迅速地擦拭咽侧壁及咽后壁数次。鼻拭子采样时,将拭子以垂直鼻子(面部)方向插入鼻孔,直至手指接近鼻子,使拭子在鼻内停留15-30秒,然后轻轻旋转3次。
取样完成后,将拭子投入专用病毒采样管中,折断拭子杆,使其完全置于管中。旋紧管盖,做好标记,放入塑料袋密封好。低温保存运输至第三方检验机构(艾迪康)进行新型冠状病毒RT-PCR检测。
1.3 统计学方法
采用SPSS20.0统计软件。计数资料采用χ2检验,P<0.05为差异有统计学意义。
2、结果
鼻、咽拭子标本各100份,其中鼻拭子取材行新型冠状病毒核酸检测阳性89例次,阳性率89%;而咽拭子取材病毒核酸阳性检出率仅为54%(54/100),结果见表1。鼻拭子标本的病毒核酸阳性率高于咽拭子采样标本,差异有统计学意义(2=3.8504,P=0.0497)。
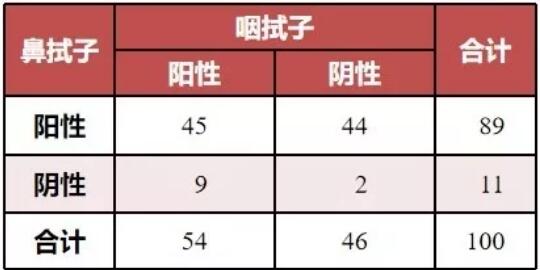
表1 新型冠状病毒肺炎100例次不同采样方式检测病毒核酸的结果比较
3、讨论
新型冠状病毒肺炎是突发的,危及全球的公共卫生事件。老年人和合并基础疾病人群患病率高,危重比例高。该病传染性强,飞沫、接触以及气溶胶均可成为该病的传播途径。因此,及时、准确地诊断该病对于控制其暴发流行以及保障人民生命安全至关重要。
在临床实践中,由于疾病暴发流行初期患者过多,病毒核酸检测能力的不足,对于该病的诊断有专家提出以胸部CT为主要判断指标。但众所周知,有关感染性疾病,病原学诊断才是金标准。故目前无论国内还是国际,仍以病人体液标本分离到新型冠状病毒核酸阳性为确诊标准。目前各种文献提出了收集患者痰液、支气管肺泡灌洗液、粪便进行核酸检查,不过无论是鼻拭子还是咽拭子进行病毒核酸检测仍是最为简便易行,更易普及的方式,也是呼吸道病毒感染或携带状态快速诊断的有效方法。
本研究比较了同一患者同时鼻拭子和咽拭子两种采样方式所取标本的病毒核酸检测结果,发现鼻拭子标本阳性率高于咽拭子标本,即病毒核酸检测敏感性鼻拭子取材效率高于咽拭子。考虑原因可能有三:
首先,本试验中鼻拭子的设计相较咽拭子可能更优。Dalmaso等[3]认为,尼龙植绒拭子上的绒毛能增加拭子与物证接触的表面积,可以最大化地转移细胞到拭子的表面,并在 DNA 提取中充分释放粘附的细胞,从而获得浓度更高的模板 DNA。Daley等[4]的研究显示,尼龙植绒拭子在转移物体表面微生物的效率比其他拭子高20%~60%。我国法医工作者的一项研究也证实了尼龙植绒拭子血痕检验的效果优于棉拭子,在微量血痕检验时优势更明显[5]。故而在病毒感染后期鼻咽部病毒较少时,此种拭子有更高的机率留取到病毒核酸。不过也有研究[6]认为,两种拭子的检验结果并无显著差异。
其次,研究发现呼吸道病毒感染病人的鼻中所带病毒可能更多于咽部。近期,广东疾病预防控制中心与中山大学团队分析了17例新型冠状病毒肺炎患者鼻部和咽部病毒载量与病程的时间关系。发现新型冠状病毒患者发病后不久就可在上呼吸道检测到较高的病毒载量。而在使用相同棉拭子进行鼻拭子与咽拭子取样后鼻腔中的病毒载量高于咽喉[7]。而另一在瑞典的研究也发现即便使用相同材质的拭子取样,鼻拭子的阳性率也几乎为咽拭子阳性率的19倍。故而即便不考虑拭子材质也推荐在呼吸道病毒采样时优选鼻拭子[8]。
其三,在新型冠状病毒肺炎的临床实践中,医护人员在采集咽拭子标本时,由于需要直接面对患者口腔,考虑到新型冠状病毒有飞沫和气溶胶形式传染途径,往往取样时间较短而且粗糙,很难采集足够标本,导致检测假阴性出现。而鼻拭子采集时医务人员处于患者侧面,医护口面部受到直接飞沫接触的机率较小,故而一般能较为仔细的采集标本。
以上几个因素可能是本研究中鼻拭子采样病毒核酸检测阳性率明显高于咽拭子的主要原因。
综上,本研究提示在临床实践中应优先考虑鼻拭子进行病毒核酸检测标本取样。这样能更多的减少漏诊,同时减少医务人员对病毒可能的暴露。当然,如能同时检测患者其他体液核酸,对新型冠状病毒肺炎患者的诊断和出院患者的监测将更有优势。
参考文献
1 . Mahony JB. Detection of respiratory viruses by molecular methods. Clin Microbiol Rev, 2008, 21(4): 716-747
2 . de la Tabla VO, Masiá M, Antequera P, et al. Comparison of combined nose-throat swabs with nasopharyngeal aspirates for detection of pandemic influenza A/H1N1 2009 virus by real-time reverse transcriptase PCR. J Clin Micro, 2010, 48(10): 3492-3495.
3 . Dalmaso G, Bini M, Paroni R, et al. Qualification of high-recovery, flocked swabs as compared to traditional rayon swabs for microbiological environmental monitoring of surfaces. PDA J Pharm Sci Technol, 2008, 62(3): 191-199.
4 . Daley P, Castriciano S, Chernesky M, et al. Comparison of flocked and rayon swabs for collection of respiratory epithelial cells from uninfected volunteers and symptomatic patients. J Clin Microbiol, 2006, 44(6): 2265-2267.
5 . 巴华杰, 金明, 王林生, 等. 尼龙植绒拭子与棉拭子血痕 DNA 分型效果比较. 中国法医学杂志, 2015, 30(3): 277-280.
6 . Brownlow RJ, Dagnall KE, Ames CE. A comparison of DNA collection and retrieval from two swab types (cotton and nylon flocked swab) when processed using three QIAGEN extraction methods. J Forensic Sci, 2012, 57(3): 713-717.
7 . Zou L, Ruan F, Huang M, et al. SARS-CoV-2 viral load in upper respiratory specimens of infected patients. N Engl J Med. 2020 Feb 19. doi: 10.1056/NEJMc2001737. [Epub ahead of print]
8 . Hernes SS, Quarsten H, Hagen E, et al. Swabbing for respiratory viral infections in older patients: a comparison of rayon and nylon flocked swabs. Eur J Clin Microbiol Infect Dis, 2011, 30(2): 159-165.
海博生物――病毒采样管(VTM运送培养基)
病毒采样管(VTM运送培养基)产品应用于各级公共卫生领域及哨点医院,用于对流感、手足口感等流行性疾病的检测采样工作,海博生物生产的病毒采样管产品2010年取得山东省青岛市食品药品监督管理局颁发的产品注册证书并推向市场,经过多年来的市场验证,已经得到广大用户的广泛认可。
检验原理:
Hank’s平衡盐构建中性环境;牛血清白蛋白做为蛋白质稳定剂与Hank’s平衡盐一起增加病毒的生存时间和感染稳定性;抗生素具有广谱抗菌的作用;苯酚红为酸碱指示剂,变色区域pH值6.6(黄)~8.0(红),在pH值7.2~7.4时呈红色。
生产备案号:鲁青食药监械生产备20150002号;
产品备案号:鲁青械备20180013号


下一篇:新冠病毒核酸检测VS抗体检测
| 相关文章: |



