

 海博微信公众号
海博微信公众号
 海博天猫旗舰店
海博天猫旗舰店


 海博微信公众号
海博微信公众号
 海博天猫旗舰店
海博天猫旗舰店




一、洁净室(区)环境监测依据
洁净实验室是指用于药品无菌或微生物检验用的洁净区域、隔离系统及其受控环境。洁净实验室的洁净级别按空气悬浮粒子大小和数量的不同参考现行“药品生产质量管理规范”分为A、B、C、D共4个级别。为维持洁净实验室操作环境的稳定性、确保检测结果的准确性,应对洁净实验室进行微生物监测和控制,使受控环境维持可接受的微生物污染风险水平。
参考GMP车间各级别洁净区空气悬浮粒子的标准表(2010年版GMP附录1无菌药品,第三章,第九条)和《中国药典》中的相关内容(9205药品洁净实验室微生物监测和控制指导原则),对照98年版GMP各级别洁净区空气悬粒子标准,洁净度级别对照关系如表1。
表1洁净区各洁净级别空气悬浮粒标准对照
|
洁净度级别 |
悬浮粒子最大允许数/m3 |
近似对应传统规格 |
|||
|
静态 |
动态 |
||||
|
≥0.5 μm |
≥5 μm |
≥0.5 μm |
≥5 μm |
||
|
A级 |
3520(ISO5) |
20 |
3520(ISO5) |
20 |
100级 |
|
B级 |
3520(ISO5) |
29 |
352000(ISO7) |
2900 |
100级 |
|
C级 |
352000(ISO7) |
2900 |
3520000(ISO8) |
29000 |
10000级 |
|
D级 |
3520000(ISO8) |
29000 |
不作规定 |
不作规定 |
100000级 |
二、监测项目
根据《中国药典》9205药品洁净实验室微生物监测和控制指导原则中的相关内容,洁净实验室应进行日常监测和定期监测,日常监测一般包括压差、温度、相对湿度等;定期监测应在风险评估的基础上建立洁净环境监测计划。定期监测内容包括物理参数、非生物活性的空气悬浮粒子数(GB/T 16292-2010)和有生物活性的微生物监测,其中微生物监测包括环境浮游菌(GB/T 16293-2010)和沉降菌监测(GB/T 16294-2010),及关键的检测台面、人员操作服表面及5指手套等的微生物监测。
在洁净实验室监控中,监测频次及监测项目建议按表2进行。例如,对于C级洁净区,需要每季度进行一次沉降菌和表面微生物监测。而对于A级洁净区,需要每次试验进行一次沉降菌和表面微生物监测。
表2推荐的洁净实验室的监测频次及监测项目
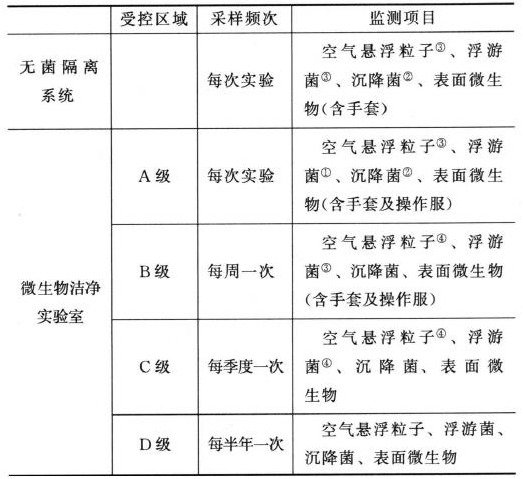
注:①每月一次。②工作台面沉降菌的日常监测采样点数不少于3个,且每个采样点的平皿数应不少于1个。③每季度一次。④每半年一次。
如果出现连续超过纠偏限和警戒限、关键区域内发现有污染微生物存在、空气净化系统进行任何重大的维修、消毒规程改变、设备有重大维修或增加、洁净室(区)结构或区域分布有重大变动、引起微生物污染的事故、日常操作记录反映出倾向性的数据时应重新评估监测程序的合理性。
三、注意事项
1、结果分析
应正确评估微生物污染,不仅关注微生物数量和种类,更应关注微生物污染检出的频率,通常在一个采样周期内同一环境中多点发现微生物污染,可能预示着风险增加,应仔细评估。几个位点同时有污染的现象也可能由不规范的采样操作引起,所以在得出环境可能失控的结论之前,应仔细回顾采样操作过程。在污染后的几天对环境进行重新釆样是没有意义的,因为采样过程不具有可重复性。
2、偏差处理
当微生物监测结果超出纠偏限度时,应当按照偏差处理规程进行报告、记录、调查、处理以及采取纠正措施,并对纠正措施的有效性进行评估。
3、微生物鉴定
建议对受控环境收集到的微生物进行适当水平的鉴定,微生物菌群信息有助于预期常见菌群,并有助于评估清洁或消毒规程、方法、清洁剂或消毒剂及微生物监测方法的有效性,尤其当超过监测限度时,微生物鉴定信息有助于污染源的调查。关键区域分离到的菌落应先于非关键区域进行鉴定。微生物鉴定参照微生物鉴定指导原则(指导原则9204)进行。
4、微生物控制
为了保证药品洁净实验室环境维持适当的水平,应保持空调系统的良好运行状态,对设施进行良好维护,洁净室内人员应严格遵守良好的行为规范,并定期进行环境监控。微生物控制措施还包括良好的清洁和卫生处理,应定期对洁净实验室进行清洁和消毒,应监测消毒剂和清洁剂的微生物污染状况,并在规定的有效期内使用,A/B级洁净区应使用无菌的或经无菌处理的消毒剂和清洁剂。所釆用的化学消毒剂应经过验证或有证据表明其消毒效果,其种类应当多于一种,并定期进行更换以防止产生耐受菌株。不得用紫外线消毒代替化学消毒。必要时,可釆用气体、熏蒸等适宜的方法降低洁净区的卫生死角的微生物污染,并对消毒剂的残留水平进行验证。
注:本文属海博生物原创,未经允许不得转载。
上一篇:胰蛋白酶溶液的生产工艺及测定标准
下一篇:黄曲霉危害及预防措施
| 相关文章: | ||



