甲型流感病毒常见培养方法与病毒拯救、扩毒技术
刘志鹏
录入时间:2026/5/13 16:35:45
来源:青岛海博生物
一、甲型流感病毒生物学特性与培养易感体系
甲型流感病毒隶属于正黏病毒科,基因组由8个独立的负链RNA节段组成,分别编码PB2、PB1、PA、HA、NP、NA、M、NS等结构蛋白与非结构蛋白,其复制过程依赖宿主细胞核,且血凝素HA的切割活化需外源性胰酶参与,这一特性决定了其体外培养的特殊条件要求。
1.病毒增殖的核心特性
与普通细菌、真菌快速增殖不同,甲型流感病毒为严格细胞内寄生,增殖高度依赖宿主细胞的合成系统。在适宜宿主体系中,病毒吸附、侵入、复制、装配与释放周期约6小时―8小时,可快速引发宿主细胞损伤。同时,病毒易发生抗原漂移与抗原转换,对培养体系的稳定性与无菌性提出更高要求,避免因污染或培养条件波动导致病毒变异、滴度下降或实验失效。
2.主流培养易感体系
甲型流感病毒的体外培养以SPF鸡胚培养与哺乳动物细胞培养为两大核心体系,二者适用场景、增殖效率与操作成本差异显著。
(1)SPF鸡胚:9日龄―11日龄无特定病原体鸡胚是病毒培养的经典天然宿主,尿囊腔与羊膜腔富含敏感上皮细胞,能为病毒提供完整的复制微环境,增殖效率高、成本可控,是疫苗生产与临床分离的首选体系。
(2)传代细胞系:以MDCK犬肾细胞为代表,其次为Vero、A549等细胞,其中MDCK细胞对甲型流感病毒敏感性高、分离阳性率稳定,可通过添加TPCK 胰酶支持病毒完整复制周期,适合实验室基础研究与快速分离。Vero细胞为非肿瘤细胞系,安全性高,多用于人用疫苗的规模化生产。
二、甲型流感病毒常见培养方法
甲型流感病毒体外培养以鸡胚培养法与细胞培养法为主,二者互为补充,共同满足基础研究与产业化需求。
1.鸡胚培养法
鸡胚培养是甲型流感病毒分离与扩增最传统、应用最广泛的方法,具备操作简便、病毒滴度高、无需复杂细胞培养条件等优势,广泛用于临床样本分离、疫苗毒种扩繁及抗原制备。
(1)鸡胚筛选与预处理:选取9日龄―11日龄SPF鸡胚,照蛋检查胚胎活力与血管分布,标记气室与接种位点,用碘伏、酒精对蛋壳表面逐级消毒,避免外源微生物带入。
(2)病毒接种:临床样本或种子病毒经无菌处理后,以尿囊腔接种为首选,每胚接种0.2 mL,低致病性病毒可采用羊膜腔接种以提升分离率;接种后用石蜡密封针孔,减少污染与水分蒸发。
(3)培养与观察:置于33℃―35℃恒温培养,相对湿度40%―60%,每日照蛋观察胚胎存活情况,弃去24小时内死亡的非特异性死亡胚。
(4)病毒收获:培养48小时―72小时后,收获存活鸡胚的尿囊液,4℃静置降温后无菌收集,低温保存备用。收获液可通过血凝试验快速判定病毒增殖效果。
2.细胞培养法
细胞培养法重复性好、易于观察病变、适合基因操作,是当前实验室研究的主流方式,其中MDCK细胞培养应用最广。
(1)细胞准备:MDCK细胞以含10%胎牛血清的DMEM或MEM培养基培养,置于37℃、5%CO2培养箱中扩增至单层汇合度80%―90%,弃培养基,PBS洗涤2次去除残留血清。
(2)病毒接种与吸附:用无血清培养基稀释病毒液,按MOI=0.01―MOI=0.1接种,37℃吸附1小时―1.5小时,期间轻摇培养瓶保证充分吸附。
(3)维持培养:弃病毒吸附液,加入含TPCK 胰酶的无血清维持液,胰酶可切割HA蛋白,保障病毒有效释放与扩散;33℃―35℃继续培养。
(4)收获与鉴定:培养48小时―72小时,显微镜下观察细胞圆缩、空泡化等细胞病变效应,收获上清液,低温离心去除细胞碎片,用于后续实验。
三、甲型流感病毒反向遗传病毒拯救技术
反向遗传技术是实现感染性甲型流感病毒人工构建的核心手段,突破了天然病毒分离的限制,可精准开展基因突变、重配疫苗株构建及功能研究,目前8质粒双向表达系统为全球通用标准方案。
1.技术原理
将甲型流感病毒8个基因组节段分别克隆至同一双向表达载体,该载体同时整合RNA聚合酶Ⅰ(PolⅠ)与RNA聚合酶Ⅱ(PolⅡ)启动子/终止子元件:PolⅠ驱动转录产生vRNA,PolⅡ驱动转录产生mRNA并翻译病毒蛋白,二者在同一细胞内协同完成病毒基因组复制与蛋白表达,最终组装出具有感染性的完整病毒颗粒。
2.病毒拯救核心流程
(1)重组质粒构建:分别扩增病毒8个基因片段,定向克隆至双向表达载体,测序验证序列正确性,确保无突变、无移码。
(2)细胞共转染:将8种重组质粒等摩尔比混合,采用脂质体转染法共转染293T细胞或293T MDCK混合细胞,转染后培养6小时―8小时,更换含胰酶的维持液。
(3)病毒拯救与传代:转染后48小时―72小时收集细胞上清,接种至MDCK细胞或SPF鸡胚进行盲传,提高拯救成功率,消除初始滴度偏低的问题。
(4)拯救病毒鉴定:通过HA试验、RT PCR、基因测序及免疫荧光等方法,验证拯救病毒的基因型、血凝活性与抗原性,确认病毒拯救成功。
3.技术应用价值
反向遗传拯救可快速实现疫苗株重配、定点突变、标记病毒构建等,大幅缩短疫苗研发周期,是应对新型流感变异株的关键技术,同时为病毒致病机制、宿主因子筛选提供可控的研究模型。
四、甲型流感病毒扩增(扩毒)与滴度定量方法
病毒扩增是获取高滴度病毒液的核心步骤,滴度测定则是量化病毒含量、保障实验一致性的关键环节。
1.病毒扩毒方法
(1)鸡胚扩毒:取种子病毒尿囊液10倍梯度稀释,接种9日龄―11日龄SPF鸡胚,33℃―35℃培养48小时―72小时,收获尿囊液,合并同批次阳性收获液,测定血凝价,通常可达到28―212,满足疫苗生产与动物实验需求。
(2)细胞扩毒:采用MDCK或Vero细胞大规模培养,以低MOI接种,维持胰酶浓度与培养温度,连续传代1―2次,收集上清液,浓缩后可用于蛋白纯化、抗体制备等。
2.病毒滴度定量检测
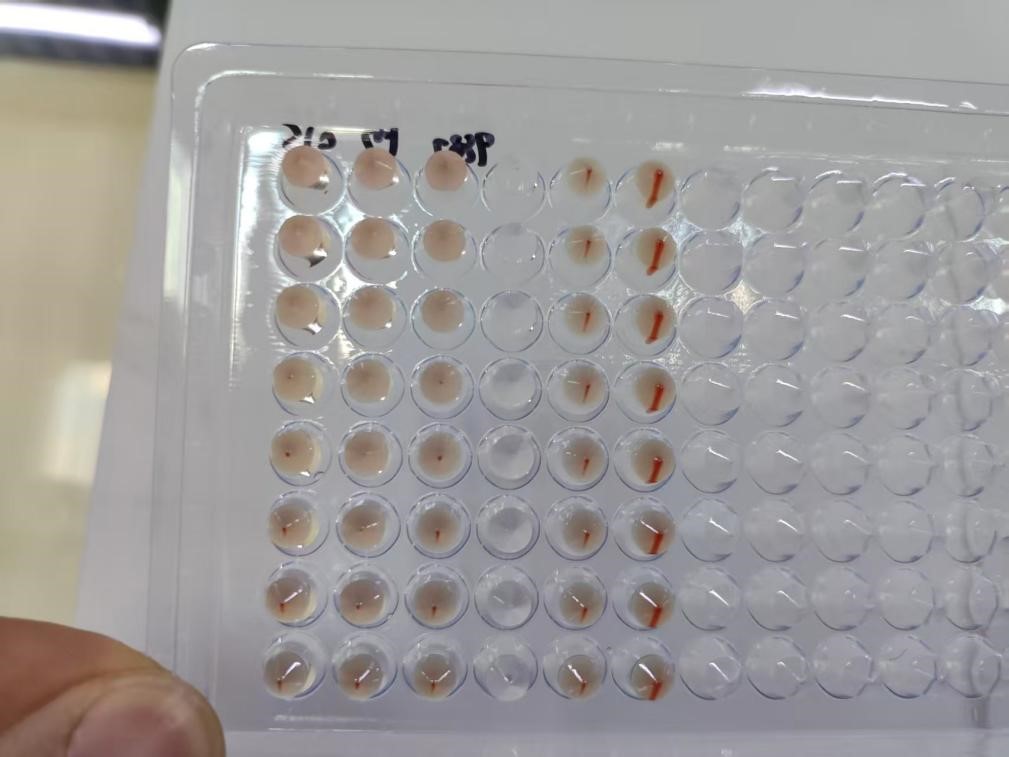
(1)血凝试验:快速初筛方法,利用病毒HA蛋白凝集鸡红细胞的特性(如图1),判定病毒存在与否,操作简便、耗时短,适合批量样本筛查。
图1 血凝试验
(2)TCID50测定:将病毒10倍梯度稀释,接种MDCK细胞单层,培养后观察CPE,采用Reed Muench法计算50%组织细胞感染剂量,反映细胞水平的病毒感染性滴度。
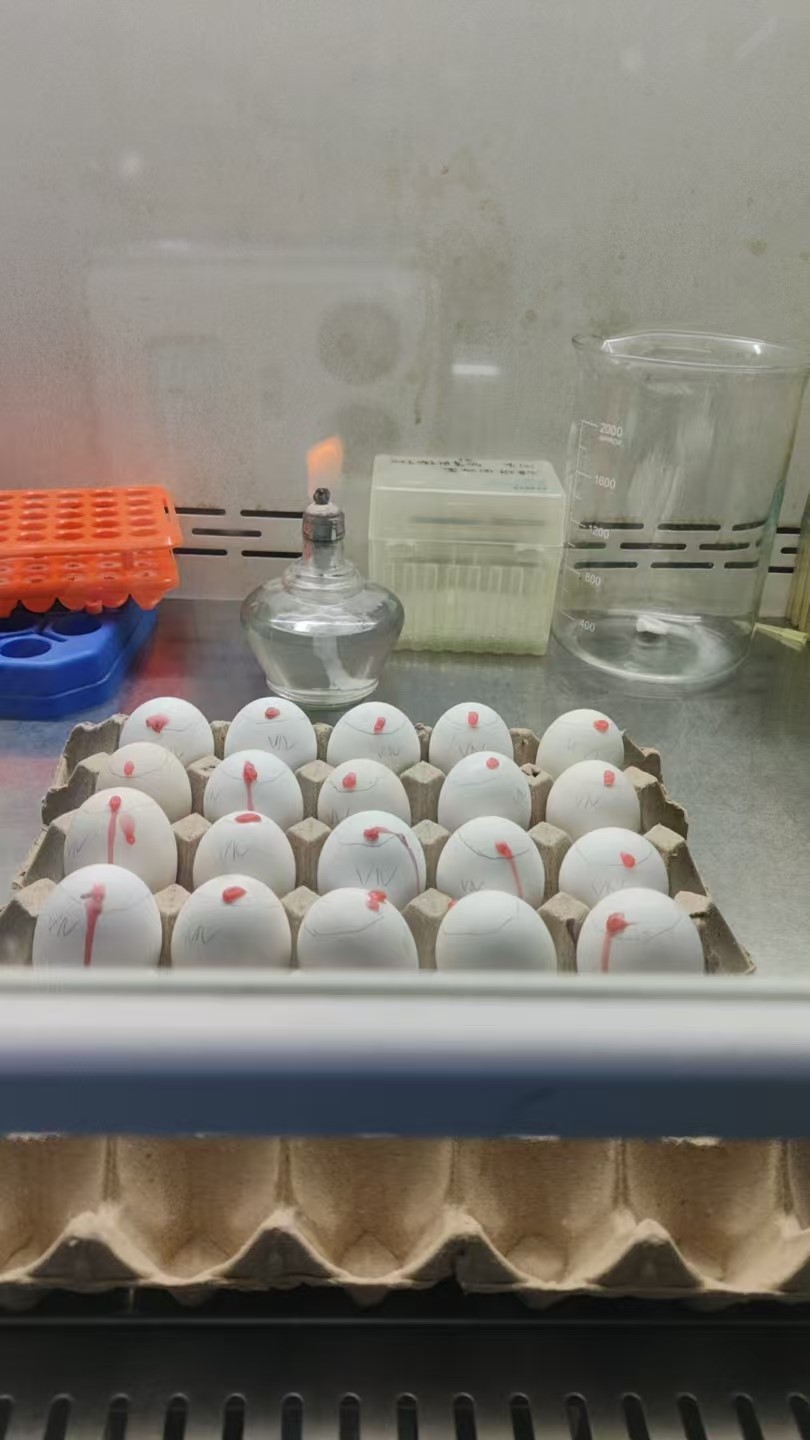
(3)EID50测定:病毒梯度稀释后接种鸡胚(如图2),培养后检测尿囊液血凝活性,计算50%鸡胚感染剂量,是疫苗质量控制的法定检测方法之一。
图2 鸡胚接种示意图
(4)空斑试验:病毒感染细胞后加入琼脂糖覆盖层,形成肉眼可见空斑(如图3),计数空斑数量计算空斑形成单位(PFU),结果精准、可定量,多用于病毒感染性精确测定。
图3 空斑实验
五、病毒培养过程的污染防控与生物安全
甲型流感病毒培养体系营养丰富、温度适宜,易受细菌、真菌、支原体污染,同时病毒本身具有致病性,需兼顾无菌控制与生物安全双重要求。
1.常见污染类型与防控措施
(1)细菌/真菌污染:表现为培养基混浊、pH骤变、出现絮状沉淀或菌丝,防控核心为严格无菌操作、使用SPF级鸡胚与无菌细胞耗材、培养基添加适量青霉素 链霉素。
(2)支原体污染:隐匿性强,无明显混浊但抑制病毒增殖,需定期用PCR法检测细胞与血清,使用支原体清除试剂,避免交叉污染。
(3)设备与环境管控:CO2培养箱、生物安全柜、水浴锅定期消毒,鸡胚操作在二级生物安全柜内完成,降低气溶胶污染风险。
2.生物安全规范
实验室需达到BSL 2级以上,高致病性禽流感病毒需在BSL 3级实验室操作;实验人员穿戴防护服、口罩、护目镜,严格执行操作规范;实验废弃物高压灭菌后处理,防止病毒泄漏与环境传播。
六、结语
甲型流感病毒的体外培养、反向遗传拯救与规模化扩毒是流感研究与防控的核心技术体系。鸡胚培养法成熟稳定、适合产业化应用,细胞培养法精准可控、适配基础研究,反向遗传技术则实现了病毒的人工精准构建。在实际操作中,需严格遵循无菌规范、优化培养参数、严控生物安全,才能保障病毒增殖效率、滴度稳定性与实验数据可靠性。随着细胞悬浮培养、反向遗传优化等技术不断进步,甲型流感病毒的培养与改造将更高效、安全,为流感疫苗迭代、药物研发及疫情应对提供更坚实的技术支撑。
注:本文属海博生物原创,未经允许不得转载。
上一篇:干酪乳杆菌简单介绍
下一篇:没有了!


 海博微信公众号
海博微信公众号
 海博天猫旗舰店
海博天猫旗舰店


 海博微信公众号
海博微信公众号
 海博天猫旗舰店
海博天猫旗舰店